中文摘要 转化生长因子β(transforming growth factor-β,TGF-β)是一种多效性细胞因子,属于调节细胞生长和分化的TGF-β超家族。在肿瘤发展的后期,自分泌和旁分泌的TGF-β可能通过诱导上皮-间质转化、促进肿瘤血管生成、调节免疫抑制来调控肿瘤的转移和复发。因此,TGF-β被认为是晚期肿瘤生长、进展和转移潜能的重要因素。中和或阻断TGF-β是一种干预和干扰肿瘤生长关键启动子的独特方法,可能会提供一个新的治疗机会。此文就TGF-β的结构、功能及其在肿瘤微环境中的作用机制进行综述,并列举了一些在研的靶向TGF-β药物,旨在为抗肿瘤药物的开发和临床应用提供参考。
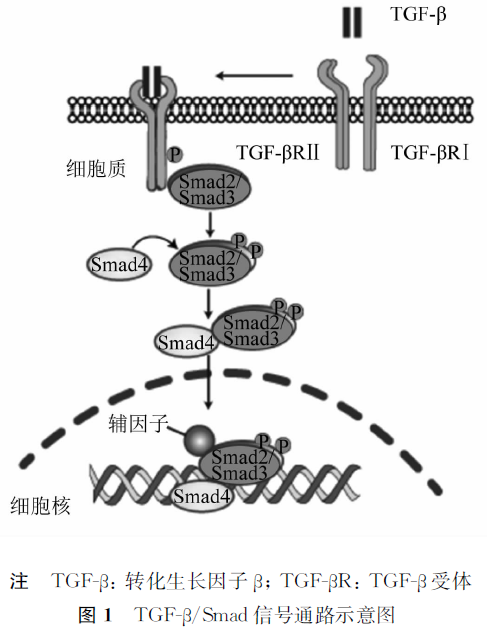
正文 肿瘤微环境是肿瘤细胞在机体内赖以生存的局部组织环境[1],包括肿瘤细胞周围的各种细胞(内皮细胞、免疫细胞、成纤维细胞等)和各种细胞外组分(细胞外基质、细胞因子、激素等)。它们围绕在肿瘤细胞周围,由血管网滋养,并相互作用,共同阻碍机体对肿瘤细胞的免疫杀伤作用,从而促进肿瘤的增殖、恶化和转移[2]。作为一种多功能细胞因子,肿瘤微环境中的转化生长因子β(transforming growth factor-β,TGF-β)在众多恶性肿瘤的发生、发展和转移中都发挥了至关重要的作用,越来越多的证据表明其具有成为肿瘤免疫治疗靶点的潜力。本文对TGF-β的结构、功能及其靶向药物研究进展等进行综述,为靶向TGF-β抗肿瘤药物的研发提供参考。 1 TGF-β及信号通路概述 TGF-β家族庞大,自1978年首次分离获得该家族第一个成员TGF-β以来,迄今已有TGF-β的5种亚型、抑制素/激活素、骨形态发生蛋白和抗穆勒管激素等家族成员被相继发现[3]。其中,TGF-β是该家族中研究较多的一种多功能细胞因子。TGF-β是相对分子质量为25 000的同源二聚体,由2个相对分子质量为12 500的亚基通过二硫键连接而成[4]。TGF-β不同亚型在物种间的分布略有不同,TGF-β1、TGF-β2、TGF-β3在哺乳动物中高度保守,编码基因具有70%~80%同源性,被认为出现在后生动物进化的早期[5];TGF-β4和TGF-β5目前研究较少,主要存在于鸟类和两栖类动物体内。由于包括大多数免疫细胞在内的几乎所有细胞均分泌潜伏形式TGF-β1[6-7],且TGF-β1是肿瘤细胞中表达最高的亚型[7],故而TGF-β1是研究TGF-β的焦点。TGF-β通过自分泌或旁分泌的方式以前体蛋白质的形式表达[8],在肿瘤微环境中经过剪切其N端延迟相关肽后形成成熟肽,2个TGF-β成熟肽分子再通过形成链间二硫键最终得到具有生物活性的同源二聚体[6]。成熟的TGF-β从其潜伏形式中激活和释放,并与质膜上的受体直接结合启动信号转导的级联反应,从而引发对响应细胞的生物作用。 研究表明,发育中的胚胎和成年动物中所有类型细胞都携带TGF-β受体(TGF-β receptor,TGF-βR),共有5种亚型[9],即TGF-βRⅠ—TGF-βRⅤ。这些受体可以通过内在催化活性发出信号,也可以作为促进或抑制配体呈递给信号受体的感受器TGF-βR来发挥作用,其中表现出内在催化活性的TGF-βRⅠ和TGF-βRⅡ是ATP依赖性蛋白激酶,N端是亲水性胞外区,能识别配体的特定结构域,其次是a螺旋跨膜结构域,C端是具有激酶活性的胞内区,接受ATP并磷酸化下游底物的丝氨酸/苏氨酸位点[10];发挥调节作用的感受器TGF-βRⅢ是镶嵌在细胞膜上的糖蛋白,不直接与TGF-β结合,但能促进TGF-β与TGF-βRⅠ、TGF-βRⅡ的结合[11]。 TGF-β与受体的结合启动下游信号通路,包括Smad通路与非Smad通路。Smad蛋白穿梭于细胞质与细胞核之间,是TGF-β信号转导进核的介质蛋白。在Smad通路中,TGF-β首先与TGF-βRⅡ胞外段结合,其胞内段结合并磷酸化TGF-βRⅠ的胞内区[12],接着TGF-βRⅠ通过在其C端区域的特定丝氨酸残基处的磷酸化激活Smad2蛋白和Smad3蛋白,再招募Smad4蛋白形成Smad2/Smad3/Smad4异源三聚体复合物,该三聚体复合物通过核孔进人细胞核,继续与各种辅因子相互作用以调控TGF-β依赖的基因表达[10],见图1。除了Smad介导的经典信号通路,TGF-β也可以通过其他信号通路调控机体生理过程,包括丝裂原活化蛋白激酶通路、PI3K/Akt通路以及JAK/STAT等信号通路[13]。丝裂原活化蛋白激酶广泛存在于真核细胞内,能通过TGF-β信号通路引起细胞发生上皮-间质转化(epithelial-mesenchymal transition,EMT)[14]。PI3K/Akt通路则是TGF-βR与磷脂酰肌醇3激酶的p85亚基结合后,磷酸化并激活下游底物Akt调控基因表达,进而促进肿瘤细胞的增殖和转移。此外,激活的Akt可防止Smad3的磷酸化,从而衰减Smad3依赖性信号传导。JAK/STAT信号通路中信号转导和转录激活因子3(signal transduction and activator of transcription 3,STAT3)被JAK激酶(与TGF-βRⅠ相互作用)磷酸化并激活,以响应TGF-β并调节TGF-β靶基因亚群的表达。在成纤维细胞中,JAK/STAT通路充当TGF-β促纤维化作用的介质[15]。TGF-β通过上述信号转导网络,对细胞增殖、分化、凋亡以及血管生成等方面产生重要影响。因此,进一步明确TGF-β对肿瘤细胞发挥的生物学功能可能在临床上为肿瘤靶向治疗提供参考。 2 TGF-β与肿瘤 肿瘤微环境中的TGF-β通过作用于肿瘤细胞及机体免疫细胞来影响肿瘤的发生、发展和转移。随着肿瘤发展进程,TGF-β表现出双重作用,即在肿瘤细胞的恶变前期,TGF-β通过抑制肿瘤细胞增殖和促进肿瘤细胞凋亡这两种途径来阻止肿瘤形成,而一旦肿瘤在机体中形成,TGF-β则通过诱导EMT、促进肿瘤新血管生成、帮助肿瘤细胞发生免疫逃逸等途径来实现肿瘤的继续发展与转移。TGF-β在肿瘤发生、发展进程中扮演双刃剑的角色,这种功能的相悖性被称为“TGF-β悖论”[16]。 2.1 TGF-β对肿瘤的抑制作用 在肿瘤形成之前,TGF-β可以通过抑制肿瘤细胞增殖和促进肿瘤细胞凋亡2种途径来发挥抗肿瘤作用。其中,抑制肿瘤细胞增殖又有2种途径:(1)TGF-β诱导细胞周期性依赖性激酶抑制因子p15、p21和p27的表达,阻止肿瘤细胞在分裂周期中由G1期向S期过渡;(2)c-Myc是参与细胞生长和分裂的主要转录因子,TGF-β通过下调c-Myc的表达,抑制肿瘤细胞分裂[17]。 TGF-β不仅可以抑制肿瘤细胞增殖,也可以通过作用于凋亡相关效应分子来促进肿瘤细胞凋亡。Humbert等[18]的实验表明在人黑色素瘤中,TGF-β能通过TGF-β/Smad信号通路诱导白血病抑制因子(leukemia inhibitory factor,LIF)分泌增加,而LIF通过磷酸化STAT3使其结合到p21启动子上从而诱导p21基因表达,后者以胱天蛋白酶3/7依赖方式诱导肿瘤细胞凋亡。此外,在原发性肝癌中TGF-β能上调死亡相关蛋白激酶的表达,诱导肝细胞发生细胞凋亡[19] ,提示增强TGF-β诱导的肿瘤细胞凋亡,可能作为肿瘤在早期阶段的治疗策略。 2.2 TGF-β对肿瘤细胞的促进作用 2.2.1 TGF-β促进肿瘤发生EMT 肿瘤形成后,肿瘤细胞通过EMT介导肿瘤的浸润转移进程。在此过程中,立方形的上皮细胞转变为狭长的纺锤体形的间质细胞,失去细胞极性,上皮细胞标志物E-钙黏蛋白减少,间质细胞标志物波形蛋白表达增加,细胞与基底膜的连接丧失,细胞流动性增加,肿瘤细胞获得向周围组织迁移、侵袭的能力[20]。EMT过程被普遍认为是肿瘤转移的根本原因,而TGF-β是几乎所有上皮组织中发生EMT必不可少的诱导因子[11]。王栋等[21]通过对食管癌细胞转染TGF-β1小干扰RNA降低TGF-β1表达,随后发现该细胞的E-钙黏蛋白表达上调,波形蛋白表达下调,且肿瘤细胞的侵袭能力降低,说明TGF-β1是促进食管癌细胞发生EMT过程的有效因子。此外,在肿瘤转移后的定植位点发生的EMT逆向过程间质-上皮转化会促进形成肿瘤转移后的病灶[22]。 2.2.2 TGF-β促进肿瘤血管生成 肿瘤的发展和转移需要经血管从宿主摄取大量的养分。肿瘤血管的生成是指在原来已存在的血管中形成密集的新血管。肿瘤微环境中的TGF-β能作用于肿瘤细胞,使之分泌血管内皮生长因子(vascular endothelial growth factor,VEGF),从而刺激内皮细胞和毛细血管腔生成,对晚期肿瘤的血管形成起到关键性作用[23]。李桃英等[24]在临床研究中发现增生期子宫内膜肿瘤患者血清中VEGF、TGF-β1的表达量均高于健康对照组女性,且恶性肿瘤组高于良性肿瘤组,同时TGF-β1表达量与VEGF呈现正相关。刘竞等[25]在人膀胱癌细胞中构建并转染TGF-β1小干扰RNA表达载体,发现VEGF表达量下调;而在高表达TGF-β1的癌细胞系中VEGF表达量随之升高。这些证据说明在肿瘤微环境中TGF-β1可能通过上调VEGF的表达来促进肿瘤新血管的生成,进而促进肿瘤发生迁移。另外,TGF-β能促进基质金属蛋白酶(matrix metalloproteinase,MMP)的表达,而MMP能够分解细胞外基质,降低细胞黏附性,增强血管内皮细胞的迁移能力,从而利于新血管生成[26]。 2.2.3 TGF-β诱导肿瘤细胞免疫逃逸 在肿瘤发生过程中,肿瘤微环境中的TGF-β可以使肿瘤细胞逃避机体免疫系统的监视。自然杀伤(natural killer,NK)细胞通过其独特的能力对肿瘤细胞做出反应,在没有适应性应答的情况下识别应激细胞,从而实现快速免疫应答。TGF-β能抑制NK细胞中的IFN-γ和T-bet表达,从而抑制Th1应答[23]。此外,树突状细胞(dendritic cell,DC)是最有效的APC,在肿瘤免疫中起着关键作用。TGF-β通过抑制MHC-Ⅱ基因的表达在体外抑制DC的抗原呈递能力。DC的耐受由TGF-β信号诱导免疫抑制分子吲哚胺2,3-双加氧酶(indoleamine 2,3-dioxygenase,IDO)和精氨酸酶介导,在乳腺癌和黑色素瘤的模型中TGF-β通过上调浆细胞类DC中的IDO和骨髓DC中的CCL22趋化因子来介导免疫逃逸[27]。与此同时,肿瘤微环境中的TGF-β能促进T细胞向调节性T细胞方向分化,进而抑制CD8+ T细胞介导的对肿瘤细胞的杀伤作用,诱导肿瘤发生免疫逃逸[28]。此外,肿瘤微环境中的TGF-β能促进巨噬细胞从具有抗肿瘤作用的M1表型向抗炎、免疫抑制的M2表型转变[11]。 3 靶向TGF-β的在研药物 鉴于TGF-β信号通路在肿瘤的发生、发展和转移过程中发挥着巨大的作用,通过抑制TGF-β的产生或者阻断其信号转导等途径以限制肿瘤进展已成为抗肿瘤治疗的一种有效手段。目前,临床上已有多种靶向TGF-β的在研药物,主要包含单克隆抗体(单抗)和TGF-βR融合蛋白、靶向TGF-β的反义寡核苷酸链及TGF-βR激酶抑制剂。 3.1 单抗和融合蛋白 Fresolimumab(GC1008)是一种人源性 IgG4抗TGF-β单抗,由1D11鼠源抗体经嵌合改造获得,可同时靶向TGF-β1、2、3,目前在晚期恶性黑色素瘤和肾细胞癌患者中进行Ⅰ期临床试验。患者在第0、28、42和56天接受静脉注射Fresolimumab,剂量递增。至少达到疾病稳定的患者可接受延长治疗,包括每2周4剂注射,最多2个额外的疗程。有29例患者接受了治疗,其中22例在剂量递增中,7例在安全队列扩展中。没有观察到剂量限制性毒性,并且确定最大剂量15 mg/kg是安全的。其中可逆性皮肤角膜棘皮瘤/鳞状细胞癌(4例患者)和角化过度的发展是观察到的主要不良事件。1例恶性黑色素瘤患者获得部分缓解,6例病情稳定,中位无进展生存期为24周[29]。 SAR439459是法国赛诺菲公司在研的一种靶向TGF-β的单抗,SAR439459单药或联合抗程序性死亡蛋白1药物西米普利单抗治疗进展期实体瘤安全性及抗肿瘤活性的临床试验正在招募患者(NCT03192345)。 LY3022859是一种抗TGF-βRⅡ单抗,在临床前评估中对乳腺癌有疗效,但Ⅰ期临床试验在14例转移性肿瘤患者中观察到不可控的细胞因子释放综合征,使试验提前终止[30]。 SRK-181是一种IgG4/kappa亚型的全人源抗体,能高特异性、高亲和力地结合TGF-β1前体复合物,但不结合TGF-β2或TGF-β3。在临床前研究中,使用SRK-181联合抗PD-1单抗治疗小鼠肿瘤模型能够让效应T细胞在肿瘤微环境中浸润并扩增,观察到持续的抗肿瘤效应[31]。同时由于高特异性,SRK-181在成年大鼠中的最大剂量增加到每周给药100 mg/kg也没有观察到药物毒性。 AVID200是一类高亲和力TGF-βRⅡ Fc融合蛋白药物,可在pmol级水平有效中和TGF-β1和TGF-β3,但不结合TGF-β2。AVID200的选择靶向性使其成为纤维化疾病和肿瘤免疫治疗中极具开发潜力的药物。目前该药已进入Ⅰ期临床研究[32]。 M7824是德国默克公司研发的一种双功能融合蛋白,能特异性地同时结合程序性死亡受体配体1(programmed death-ligand 1,PD-L1)和 TGF-β。在小鼠肿瘤模型中,M7824比用抗PD-L1抗体或TGF-β陷阱治疗能更有效地抑制肿瘤生长和转移[33]。使用M7824治疗晚期非小细胞肺癌,患者中位总生存期为17.1个月,与抗PD-1单抗治疗相比有显著延长。另外,长达3年的随访结果表明M7824对PD-L1高表达的患者具有可控的安全性,且具有较长的缓解持续时间和较好的长期临床获益[11]。但在治疗接受过免疫检查点抑制剂后疾病进展的微卫星高度不稳定/错配修复缺陷实体瘤患者的Ⅱ期临床研究(NCT03436563)中,M7824未显示出抗肿瘤活性而以失败告终,包含159例患者的M7824单药二线治疗局部晚期或转移性胆道癌的Ⅱ期临床试验也因未达到主要终点而终止。目前,M7824还有宫颈癌、乳腺癌、尿路上皮癌、非小细胞肺癌联合疗法等多项处于不同阶段的临床试验。 3.2 靶向TGF-β的反义寡核苷酸链 反义寡核苷酸链AP12009靶向沉默TGF-β2 mRNA,用于恶性黑色素瘤和胶质瘤的治疗。在难治型胶质瘤的Ⅰ/Ⅱ期临床试验中,10 μmol/L AP12009治疗组的中位生存期为12.0个月,80 μmol/L AP12009治疗组为13.1个月,标准化治疗组为11.0个月,表明AP12009可能是一种很有希望的抗肿瘤药物[34],具有较高的开发潜力。目前,AP12009已进入治疗转移性黑色素瘤、胰腺癌和转移性结直肠癌的Ⅲ期临床研究。 STP705是一种在研的靶向TGF-β1和COX-2基因的小干扰RNA治疗药物,由多肽纳米颗粒配制而成。在临床前动物模型中,STP705给药增加了T细胞对肝脏肿瘤的渗透,并增加了肝细胞癌模型中抗PD-L1抗体的疗效。在1项正在进行的评估STP705的Ⅱ期临床研究中,通过每周1次病灶内注射,共持续6周用于治疗非黑色素瘤皮肤癌,中期分析表明一些患者的病变出现组织学清除,且接受治疗的患者没有出现皮肤不良反应[35]。 3.3 TGF-βR激酶抑制剂 小分子抑制剂SB-431542能特异性结合到TGF-βRⅠ,通过抑制其激酶活性来阻断下游Smad2/3磷酸化,从而阻断TGF-β/Smad信号通路。SB-431542在恶性神经胶质瘤细胞中能够抑制血管生成,阻断肿瘤细胞的迁移作用,同时能有效抑制TGF-β诱导的人骨肉瘤细胞增殖和迁移[36]。 Galunisertib(LY2157299)是目前研究最广泛的新型口服小分子抑制剂,其作用机制与SB-431542相同,能抑制TGF-βRⅠ激酶活性[37]。Galunisertib在乳腺癌、结肠癌、肺癌和肝癌异种移植肿瘤中具有抗肿瘤活性[38]。在人体剂量研究中,56例胶质瘤患者中有12例观察到临床获益,且300 mg/d的Galunisertib安全性良好,可用于未来的临床研究[39]。 Vactosertib(TEW-7197)是处于临床开发中的TGF-βRⅠ选择性小分子抑制剂,特异性靶向TGF-βRⅠ的腺苷-5’-三磷酸结合位点,从而抑制Smad2和Smad3的磷酸化来阻断下游信号通路。Ⅰ期剂量递增研究在晚期实体瘤患者中评估了Vactosertib的安全性、有效性以及与TGF-β反应特征的相关性,患者在剂量范围内(30~340 mg)每日1次接受Vactosertib,持续5 d,休息2 d。结果表明Vactosertib的安全性和耐受性良好,但最大耐受剂量尚未确定;接受≥140 mg治疗的17例患者中有6例病情稳定(35.3%),并且成纤维细胞TGF-β反应特征比进行性疾病患者更高[40]。 4 展望 TGF-β是一种多效细胞因子,根据所处的肿瘤微环境,可以产生促肿瘤或抗肿瘤作用。在肿瘤形成后,TGF-β能通过介导EMT、促进血管生成、诱导免疫逃逸等作用来促进肿瘤细胞的生长、浸润与转移。尽管大量临床前和转化研究表明,阻断TGF-β是一种潜在有效的治疗策略,但从实验室到临床的转化进展缓慢,目前尚未有靶向TGF-β药物被批准用于癌症治疗,这可能与TGF-β的双重作用有关。阻断TGF-β信号通路,同时解除肿瘤微环境的免疫抑制,已成为目前研究靶向TGF-β药物的热门方向,而如何设计TGF-β抑制剂与免疫检查点抑制剂的联用还需要进一步思考与探索。 引用本文:马钧. 转化生长因子β在肿瘤微环境中的作用及其靶向药物研究进展 [J]. 国际生物制品学杂志, 2023, 46(2): 103-108. DOI: 10.3760/cma.j.cn311962-20220127-00009